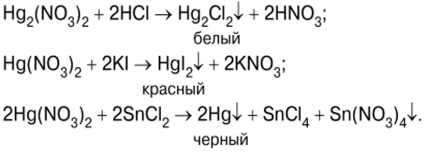
Merkurio-konposatuen erreakzioak
Merkurio metalikoa eta bere konposatuak oso toxikoak dira izaki bizidunentzat. Hau bereziki egia da uretan oso disolbagarriak diren konposatuentzat. Kontuz ibili behar da elementu berezi honen konbinazioekin esperimentatzen denean (merkurioa da giro-tenperaturan likidoa den metal bakarra). Kimikariaren oinarrizko manuak betetzea? merkuriozko konposatuekin hainbat esperimentu segurtasunez egiteko aukera emango dizu.
Lehenengo esperimentuan, aluminio-amalgama lortzen dugu (merkurio likidoan metal horren disoluzioa). Merkurio (II) disoluzioa Hg nitratoa (V) Hg (NO3)2 eta aluminiozko alanbre zati bat (1. argazkia). Aluminiozko hagatxo bat (gordailuak kontu handiz garbituta) saiakuntza batean jartzen da merkurio gatz disolbagarri baten soluzio batekin (2 argazkia). Denbora pixka bat igaro ondoren, hariaren gainazaletik gas burbuilak askatzen direla ikusi ahal izango dugu (3. eta 4. argazkiak). Hagaxka disoluziotik kendu ondoren, buztina estaldura leun batez estalita dagoela ematen du, eta, horrez gain, merkurio metalikoko bolak ere ikusten ditugu (5. eta 6. argazkiak).
Kimika - merkurioa konbinatzeko esperientzia
Baldintza normaletan, aluminioaren gainazala aluminio oxidozko geruza estu batekin estaltzen da.2O3metala modu eraginkorrean isolatzen du ingurumen-eragin oldarkorretatik. Haga garbitu eta merkurio gatz disoluzio batean murgildu ondoren, Hg ioiak desplazatzen dira2+ aluminio aktiboagoa
Hagatxoaren gainazalean metatutako merkurioak aluminioarekin amalgama bat eratzen du, eta horrek zaildu egiten du oxidoari atxikitzea. Aluminioa oso metal aktiboa da (urarekin erreakzionatzen du hidrogenoa askatzeko - gas burbuilak ikusten dira), eta egiturazko material gisa erabil daiteke oxidozko estaldura trinkoaren ondorioz.
Bigarren esperimentuan, amonio NH ioiak detektatuko ditugu.4+ Nessler-en erreaktiboa erabiliz (Julius Nessler kimikari alemaniarra izan zen analisietan erabili zuen lehena 1856an).
Lupuluaren eta merkurio-konposatuen erreakzioari buruzko esperimentua
Proba merkurio(II) ioduro HgI prezipitazioarekin hasten da.2, potasio ioduro KI eta merkurio (II) nitrato (V) Hg (NO) disoluzioak nahastu ondoren3)2 (argazkia 7):
HgI-ren prezipitazio laranja-gorria2 (8. argazkia) ondoren, potasio ioduro disoluzio gehiegizko batekin tratatu K formulako konposatu konplexu disolbagarri bat lortzeko2HgI4 ? Potasio tetraioderkuratoa (II) (9. argazkia), Nesslerren erreaktiboa dena:
Lortutako konposatuarekin amonio ioiak detekta ditzakegu. NaOH sodio hidroxidoaren eta NH amonio kloruroaren disoluzioak beharko dira oraindik.4Cl (10. argazkia). Nessler erreaktiboari amonio gatz disoluzio kopuru txiki bat gehitu eta ertain sendo batekin alkalinizatu ondoren, saio-hodiaren edukiaren kolore hori-laranja sortzen dela ikusten dugu. Uneko erreakzioa honela idatz daiteke:
Lortutako merkurio-konposatuak egitura konplexua du:
Oso sentikorra den Nessler proba uretan (adibidez, iturriko ura) amonio-gatzen edo amoniakoaren arrastoak detektatzeko erabiltzen da.

